Prêt pour le nouveau MDR avec Amoena
Le règlement sur les dispositifs médicaux (MDR) est un règlement européen relatif aux dispositifs médicaux qui est entré en vigueur fin mai 2017 (UE 2017/745). Après une période transitoire, qui a été prolongée pour des raisons de coronavirus, les exigences doivent être appliquées à partir du 26 mai 2021 au plus tard. Tant pour les fabricants de dispositifs médicaux que pour les distributeurs, des changements importants doivent être mis en œuvre au plus tard à cette échéance.
Amoena est bien préparée à l'application du nouveau règlement sur les dispositifs médicaux à partir du 26 mai. En mettant en œuvre les exigences du RIM, nous les avons rendues aussi pratiques, simples et transparentes que possible pour les deux parties - pour nous en tant que fabricant et pour nos partenaires revendeurs.
Quels sont les effets visibles du MDR ?
Selon le MDR, des informations supplémentaires sont requises pour l'étiquetage des dispositifs médicaux. À l'avenir, en plus du code qui identifie clairement les produits, vous trouverez d'autres données et symboles sur l'emballage et l'étiquette. Les produits sous la responsabilité d'Amoena Medizin-Orthopädie-Technik GmbH (distributeur et fabricant) sont reconnaissables à notre adresse derrière un symbole d'usine noir sur l'étiquette ou l'emballage :
 Amoena Medizin-Orthopädie-Technik GmbH
Amoena Medizin-Orthopädie-Technik GmbH
Kapellenweg 36, 83064 Raubling, Germany
www.amoena.com
Que se passe-t-il avec les anciens produits (voir article 120, alinéa. 4 du MDR) ?
Les produits portant des étiquettes anciennes peuvent :
- être vendus par vous en tant que détaillant spécialisé jusqu'en mai 2025,
- pour autant que la date de péremption ne soit pas dépassée avant cette date.
- Cela vaut également pour les produits qui sont arrivés dans votre entrepôt de consignation avant le 26 mai 2021. Ils sont considérés comme ayant été mis sur le marché et ne doivent pas être réétiquetés.
Quelles sont exactement les exigences en matière d'étiquetage des produits?
En plus de la marque CE bien connue, vous trouverez également de nouveaux symboles que nous souhaitons vous présenter ci-dessous :
 | Date d'expiration : À partir de la date de validité du MDR, les produits doivent contenir une date de fabrication ou de péremption. Nos produits Prothèses, Compléments Mammaires et Form Care porteront une date de péremption. La date de péremption est déterminée sur la base d'études de durée de conservation. Les produits périmés ne peuvent plus être vendus.
|
 | Date de fabrication (= date d'expédition) : À partir de la date de validité du MDR, les produits doivent comporter une date de fabrication ou de péremption. Nos soins de récupération et autres textiles porteront une date de fabrication.
|
 | Numéro de référence : Le symbole est affiché avant le numéro de l'article
|
 | Numéro de série : Le symbole est affiché avant le numéro de série
|
 | Numéro de lot de production : Le symbole est affiché avant le numéro de lot de production
|
 | Le symbole "MD" signifie dispositif médical - ce symbole est affiché pour indiquer que le produit est un dispositif médical. |
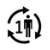 | Patient unique - usage multiple : Le produit peut être utilisé plusieurs fois par un seul patient. |
 | Pour en savoir plus, consultez le mode d'emploi : |
 | Si l'emballage est endommagé, le produit ne doit pas être utilisé. |
 | Les produits sous la responsabilité d'Amoena GmbH (fabricant) sont reconnaissables à notre adresse derrière un symbole d'usine noir sur l'étiquette ou l'emballage. |
 | Protégez les produits de la lumière du soleil |
Qu'en est-il des instructions d'utilisation ?
Dans le cas très improbable d'un "incident grave" avec un dispositif médical de notre classe de risque, le législateur nous oblige à faire référence à une obligation de déclaration dans les instructions d'utilisation. En outre, comme l'exige le MDR, vous et vos clients trouverez nos instructions d'utilisation actuelles sur notre page d'accueil au plus tard à la date limite.
Pour toute autre question concernant le MDR, n'hésitez pas à nous contacter.





 Amoena Medizin-Orthopädie-Technik GmbH
Amoena Medizin-Orthopädie-Technik GmbH








